成都理工大学继续教育培训
 咨询电话:
咨询电话:400-0815-589
欢迎来到继续教育培训网院校库!
继续教育培训网首页 咨询电话:
咨询电话:近期,以我校材料与化学化工学院教师、地质灾害防治与地质环境保护国家重点实验室固定研究人员曾庆乐教授为论文通讯作者。以硕士研究生康晓康、李福海同学作为第一作者,分别在国际化学期刊《Organic Letters》(Nature Index期刊,SCI影响因子6.005)和《Chemical Communications》(Nature Index期刊,SCI影响因子6.222)上发表研究论文。
康晓康同学在《Organic Letters》上发表的论文题目为“Water-Mediated Intramolecular Cyclization/Oxidation of α‑Carbonyl Sulfur Ylides: Synthesis of Corey−Chaykovsky Reagent Type Heterocycles”;李福海在《Chemical Communications》上发表的论文题目为“Transition metal-free coupling reactions of benzylic trimethylammonium salts with di(hetero)aryl disulfides and diselenides”。
一、康晓康同学作为一作在《Organic Letters》上发表的研究成果的简介
硫叶立德是一种碳负离子和邻近的硫正离子组成的两性离子化合物,由化学家Johnson在1961年偶然发现。后来,诺贝尔奖获得者科里和他的学生柴可夫斯基在1962年发现了亚砜叶立德,即“科里-柴可夫斯基试剂” (图1)。亚砜叶立德被广泛用于含碳-碳双键或碳-杂原子双键的酮、醛、亚胺和a,β-不饱和羰基化合物等的加成反应,合成具有三元环化合物;由于这类反应在有机化学、天然产物合成、药物合成等领域经常出现,因此,这类反应被称为 Johnson-Corey-Chaykovsky反应(图1)。虽然科里-柴可夫斯基试剂在有机合成、药物化学和天然产物合成中得到了广泛的应用,但只有少数环状亚砜叶立德被报道,并且未见带有亚砜叶立德结构的杂环的报道。如果能够实现亚砜叶立德结构杂环的合成,就会拓展有机化学的研究领域。
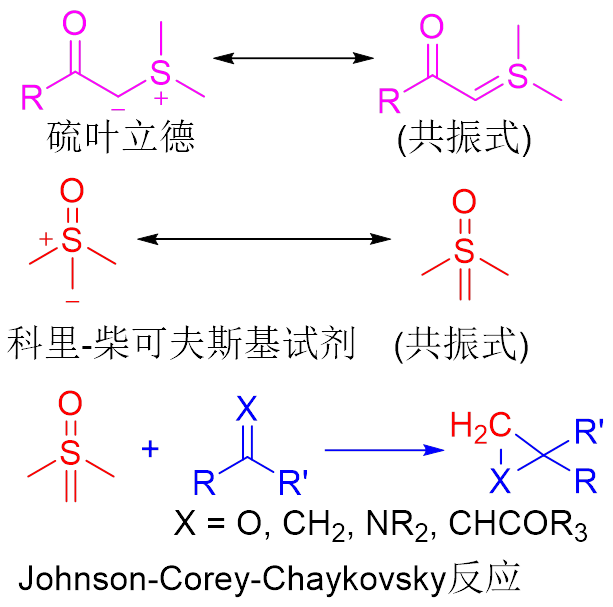
图1. 硫叶立德、科里-柴可夫斯基试剂和Johnson-Corey-Chaykovsky反应
在实验研究中,曾庆乐课题组偶然发现由苯甲酰亚甲基二甲基锍盐原位生成的α-羰基硫叶立德在水和乙腈的混合溶液中发生新奇的分子内环化/氧化反应(图2),得到一类含亚砜叶立德结构的五元杂环新类型化合物。
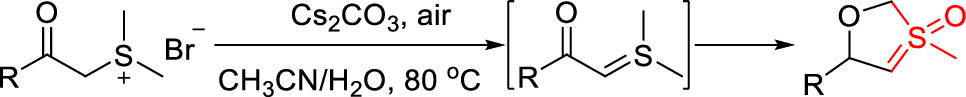
图2. 本研究发现的新反应
为了探究反应的适用范围,本研究进行了底物拓展,实验结果表明(图3),此反应对于底物是缺电子的芳烃时产率较低,但苯环上若带有给电子的取代基如甲氧基、甲基时反应产率较高。遗憾的是,脂肪类的二甲基溴化锍不反应。
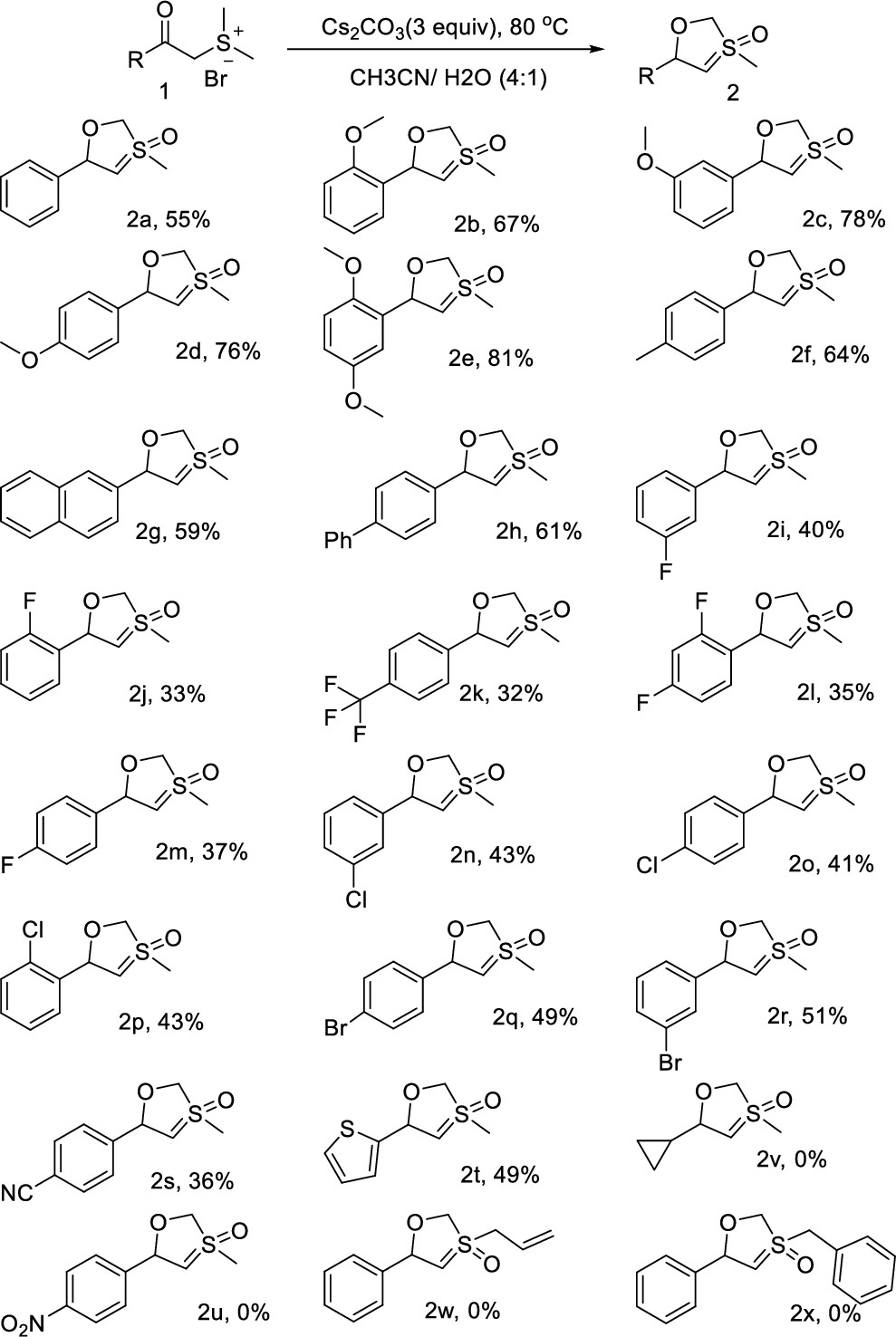
图 3. 反应底物的适用范围
为了探究反应机理,进行了控制实验和D2O和H218O标记实验的研究。根据控制实验研究结果,曾庆乐课题组提出一种由水参与的、sp3碳氢键和羟基氧化偶联反应引起分子内环化的反应机理(图4)。
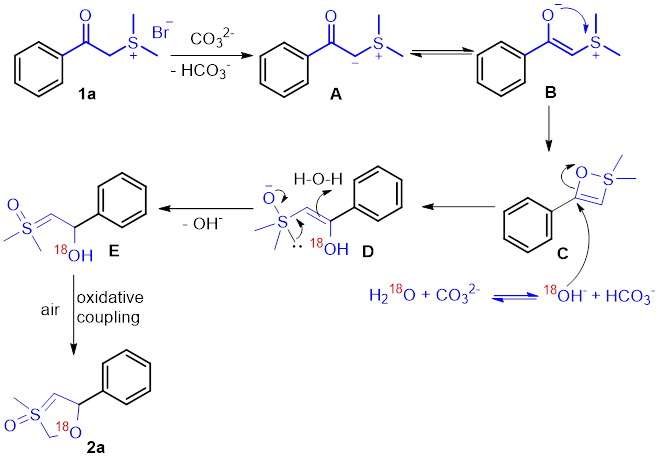
图4. 推导的反应机理
该论文发表后,收到广泛关注。国际有机合成期刊Synthesis主编、著名化学家Paul Knochel教授邀请曾庆乐课题组在Synthesis发表Feature Article。
该研究工作得到了地质灾害防治与地质环境保护国家重点实验室(No. SKLGP2020Z003)和成都市科技局(2019-YF05-02395-SN)的资助。
文章链接:https://doi.org/10.1021/acs.orglett.1c02667
二、李福海同学作为一作在《Chemical Communications》上发表的研究成果的简介
许多含硫醚、硒醚结构的化合物显示出重要的生物活性。目前合成硫醚、硒醚的方法是通过过渡金属催化恶臭、毒性较大的硫醇、硫酚、硒酚等的C–S偶联反应来合成。过渡金属参与的反应,在后处理纯化阶段难以完全除去过渡金属,增加纯化成本;纯化不到位,又存在产品(例如药物)毒性隐患。
季铵盐作为一种新型的亲电试剂,性质稳定,无特殊气味,可以在无金属条件下与二硫(硒)化物,高效构建普通硫醚、硒醚等化合物。不仅如此,采用具有手性的季铵盐作为亲电试剂,还可以手性保留得到具有手性的硫醚、硒醚等重要结构。此策略绿色无污染,对环境友好,在药物合成领域具有十分重要的意义。
在长期研究有机硫族化学基础上,曾庆乐课题组发现无过渡金属催化的苄位硫醚(硒醚)的合成方法(图5)。苄位三甲基季铵盐在碳酸铯的作用下,在乙腈中分别与二芳基二硫化物、二硒化物反应,得到苄位硫醚、苄位硒醚。
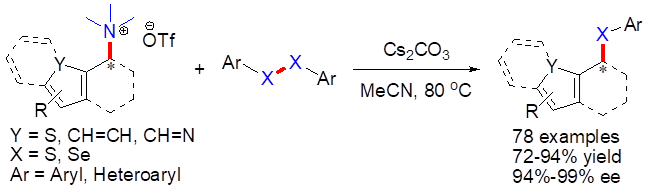
图5. 无过渡金属催化的C-S键、C-Se键偶联反应合成(手性)苄位硫醚、硒醚
对非手性苄位季铵盐的底物范围进行了考察,并对各类二硫化物和二硒化物也进行了扩展,各类取代基的底物都能适应,并且杂环的季铵盐和二硫(硒)醚也有较好的产率(图6)。

图6. 底物适用范围
更重要的是,该反应也适用于手性苄位季铵盐,并且原料苄位季铵盐的手性在产物中保留良好(94–99% ee)(表1);而且,反应过程中,手性构型发生翻转,即产物的构型跟原料的构型正好相反。
表1. 手性苄位季铵盐和二苯基二硫化物、二硒化物的反应结果
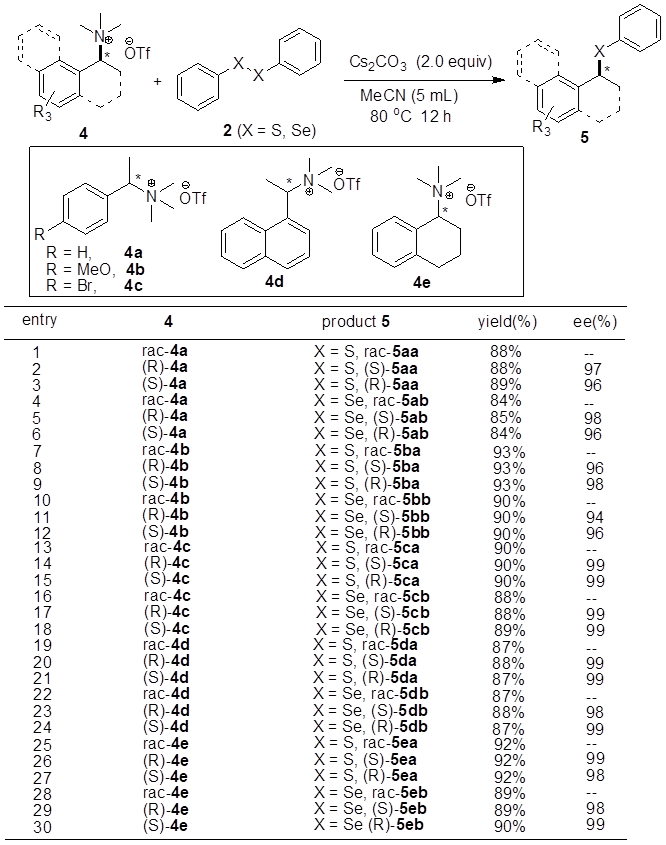
最后,我们做了控制实验研究,提出了一种协同作用的反应机理,其中手性的翻转是通过SN2型的取代反应过程实现的(图7)。
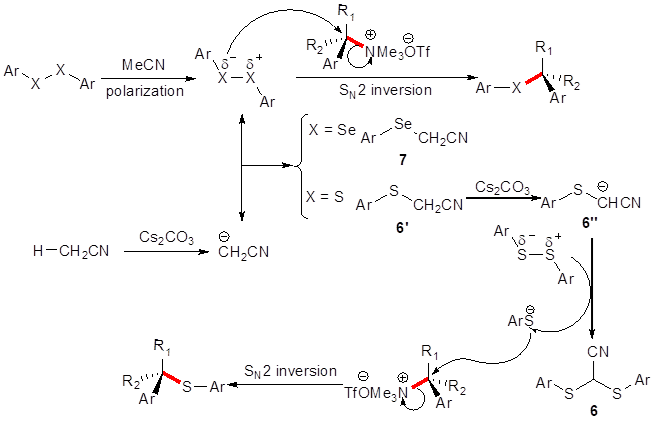
图7. 可能的反应机理
本论文的方法为合成苄位硫醚和苄位硒醚提供了一种新的路线。该方法目前是最有效的苄位手性硒醚合成方法,且具有以下优点:无需金属催化,反应条件较为温和,底物适用范围广,后处理简便,产率普遍较高(72–94%),手性产物具有优异的对映体纯度(94–99% ee)。
与该研究工作的相关研究,曾庆乐课题组已经在ACS Catal.、J. Org. Chem.、Asian J. Org. Chem.、Eur. J. Org. Chem.、Chem. Rec.等期刊上发现一系列的学术论文,并受到国际关注,例如,ACS Catal.在短短三年内已经被SCI引用40次。
该论文得到国家自然科学基金(No. 21372034)和地质灾害防治与地质环境保护国家重点实验室(No. SKLGP2018Z002)的经费资助。
文章链接:https://doi.org/10.1039/D0CC05633B
