 咨询电话:
咨询电话:400-0815-589
欢迎来到继续教育培训网院校库!
继续教育培训网首页近日,中国海洋大学海洋生命学院、海洋生物多样性与进化研究所王岩教授研究组在海洋微生物生态感知与响应领域取得系列研究成果。研究论文“Novel indole-mediated potassium ion import system confers a survival advantage to the Xanthomonadaceae family”发表于微生物生态学顶级期刊The ISME Journal。研究论文“MomL inhibits bacterial antibiotic resistance through the starvation stringent response pathway”发表于mLife(中国科技期刊卓越行动计划高起点新刊)。研究论文“Developing a new treatment for superficial fungal infection using antifungal collagen-HSAF dressing”发表于生物学顶级期刊Bioengineering and Translational Medicine。
海洋微生物对生态信号的感知与响应,是其能够参与多种生物海洋学过程的重要因素,具有明显的研究意义。研究表明,种间信号分子吲哚能够增强产酶溶杆菌LeYC36的抗高渗透压能力。在产酶溶杆菌LeYC36中鉴定了一种新的钾离子摄入系统LeKdpXFABC,信号分子吲哚被细胞识别后,可以通过两种响应方式增强该系统对钾离子的摄入。一种是通过双组分QseC/QseB直接诱导LekdpXFABC操纵子的高效表达,进而增强细胞对钾离子的摄入来提高抗高渗透压的能力;另一种响应方式是通过促进细胞膜上脂多糖的合成将更多钾离子吸附到细胞膜上,协助LeKdpXFABC系统对钾离子的摄入。产酶溶杆菌通过感知异己细菌释放的吲哚增强自身抗高渗透压能力,提高了生存优势,同时稳定产出多种胞外裂解酶,降解更多的胞外有机物为异己细菌提供营养。本研究为更全面的解析复杂环境中微生物的通讯互作和互惠共生模式提供新的理论素材。研究论文发表于The ISME Journal,中国海洋大学王岩教授为本论文的通讯作者,刘光磊教授、龙红岸教授和韩勇助理教授参与了本项工作。中国海洋大学为第一通讯单位。
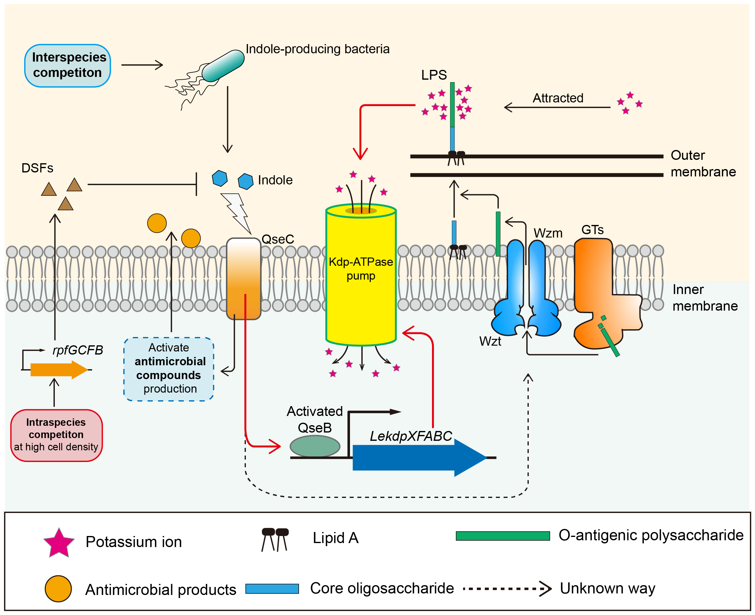
图1. 吲哚介导的产酶溶杆菌LeYC36钾离子摄入通路图
N-酰基高丝氨酸内酯(AHLs)信号分子在调控细菌耐药性、被膜合成、毒力因子表达等生理行为中发挥重要作用。海洋来源的群体感应淬灭酶MomL对AHLs有显著降解能力,可通过新型通路las-relA-rpoS-H2-T6SS来调控细菌对环境抗生素的感知与代谢能力,该过程与relA介导的饥饿反应(Starvation Stringent Response)高度相关。本研究基于信号分子对细胞的级联调控途径,阐明了AHLs的新型感知与淬灭模式,明确了MomL对细菌感知与代谢环境抗生素的调控机制,为更充分地解析微生物对信号分子的感知与响应过程提供了现实素材及理论依据。该研究发表于中国科技期刊卓越行动计划高起点新刊mLife上,并入选创刊号。中国海洋大学王岩教授、张晓华教授以及中山大学袁进教授为本论文的通讯作者,中国海洋大学于日磊教授、龙红岸教授、王祥红教授参与了本项工作。中国海洋大学为第一通讯单位。
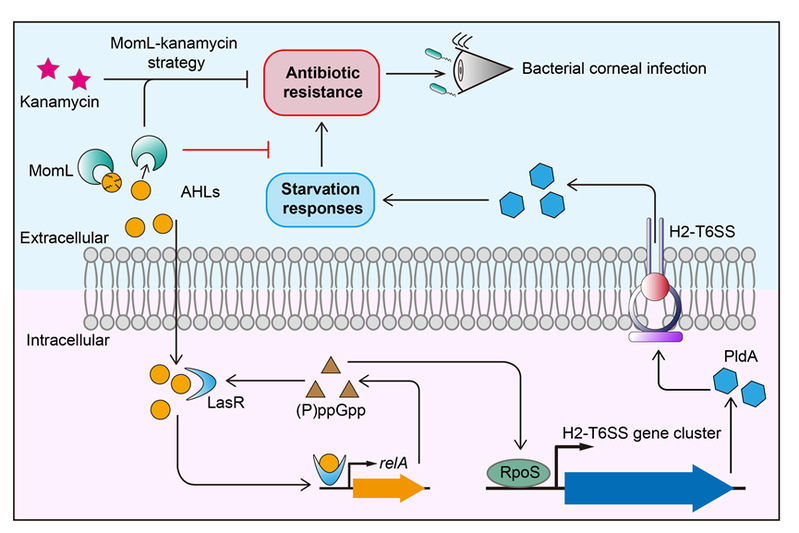
图2. MomL淬灭AHLs介导的种间互作机制
另外一项研究中,发现信号分子吲哚可诱导产酶溶杆菌LeYC36的抗菌物质提前表达,促使其生物合成基因簇在细菌生长初期便被激活。从吲哚调控生物合成的视角阐释了海洋环境中的微生物间竞争机制,并将这种机制延伸至抗菌领域。本研究发表于Bioengineering and Translational Medicine,中山大学袁进教授和中国海洋大学王岩教授为本论文的通讯作者,杜良成教授和李瑶瑶副教授参与了本项工作。
研究工作得到了国家自然科学基金、中国科协青年人才托举工程、山东省青年泰山学者、山东省重大科技创新工程等项目的资助。
