咨询电话:
咨询电话:400-0815-589
欢迎来到继续教育培训网院校库!
继续教育培训网首页7月16日,《Cell Reports》杂志在线发表了我校焦新安教授研究团队的最新研究论文“Salmonella Coiled-Coil- and TIR-Containing TcpS Evades the Innate Immune System and Subdues Inflammation”。该论文研究了沙门菌TcpS通过干扰TLR-NFκB信号通路来发挥抑炎功能的分子机制,揭示了沙门菌免疫逃逸的新策略;通过评价TcpS的功能性肽段在过度炎性反应中的抑炎效应,为新型抑炎小分子药物的设计提供了新思路。
沙门菌是一类重要的人兽共患病原菌,对畜禽养殖业危害严重,亦可引起公共卫生问题,因此,对沙门菌感染和免疫机制的研究意义重大。
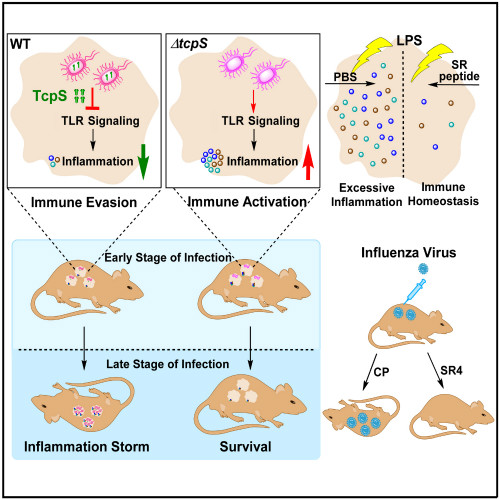
该研究团队在沙门菌中鉴定了含有Coiled-coil和TIR结构域的基因tcpS,确定了肠炎沙门菌可通过T3SS1分泌TcpS蛋白。TcpS通过模拟TLRs的TIR结构域干扰TLR-NFκB信号通路,抑制p65的入核以及炎性细胞因子的分泌,从而逃逸天然免疫应答。另外,肠炎沙门菌在感染早期抑制炎症反应,促进其在体内的增殖,最终导致其在感染后期引起血液中炎性风暴,造成组织病理损伤。TcpS通过N端的Coiled-coil结构域形成同源二聚体,是TcpS发挥高效抑炎作用所必需的。该研究还进一步确定了TIR-TcpS多肽可抑制LPS诱导的炎性因子的产生、 p-ERK和p-JNK的活化、降低小鼠血清中炎性反应和血红蛋白的释放。SR4多肽在H1N1流感病毒攻毒模型中对小鼠具有良好的保护效应,进一步确定了TcpS蛋白中关键的功能性肽段,其可作为过度炎性反应或自身免疫性疾病的潜在治疗药物。本研究揭示了肠炎沙门菌逃逸机体天然免疫的新机制,亦为沙门菌减毒活疫苗和新型抑炎小分子药物的设计提供了新思路。
我校博士研究生熊丹为论文第一作者,焦新安教授、潘志明教授为论文共同通讯作者。我校徐秀龙教授和伊利诺伊大学芝加哥分校孙俊教授在论文指导和数据分析上提供了重要帮助。本研究得到国家自然科学基金和国家重点研发计划等项目资助。